
差式扫描微量热DSC精确测量主动加热过程中,蛋白去折叠过程中吸收的热量。从而获得关于蛋白稳定性相关的一系列精细指标,以判断不同形态(或不同来源)生物分子之间的稳定性差异或相似性。

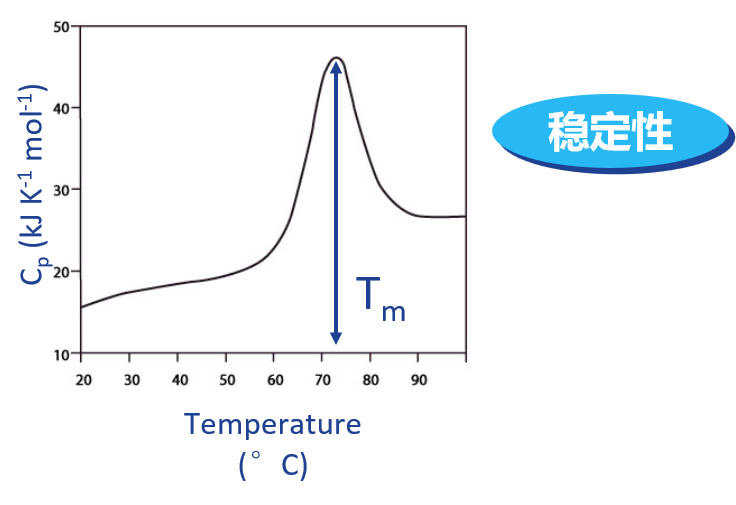
蛋白质在恒定加热速率的加热过程中发生去折叠,并伴随着热量的变化。差示 DSC通过精确测量该过程中热容的变化,从而对蛋白质的稳定性进行直接的度量和比较。DSC 提供的转变中点温度(Tm)被认为是判断蛋白质稳定性的重要指标,在诸如生物药物的开发和剂型研究过程中能够快速、直接地提供蛋白质或剂型的稳定性依据。例如定点突变提高了蛋白质的 Tm 值,从而具有更高的热稳定性。而这种热稳定性与蛋白质的长期稳定性具有良好的一致性,能够更早地对蛋白质的保存时效进行预测和优化。
DSC 也可以应用于相互作用研究中:分子相互作用通常会造成蛋白质趋于稳定和 Tm值的提高。
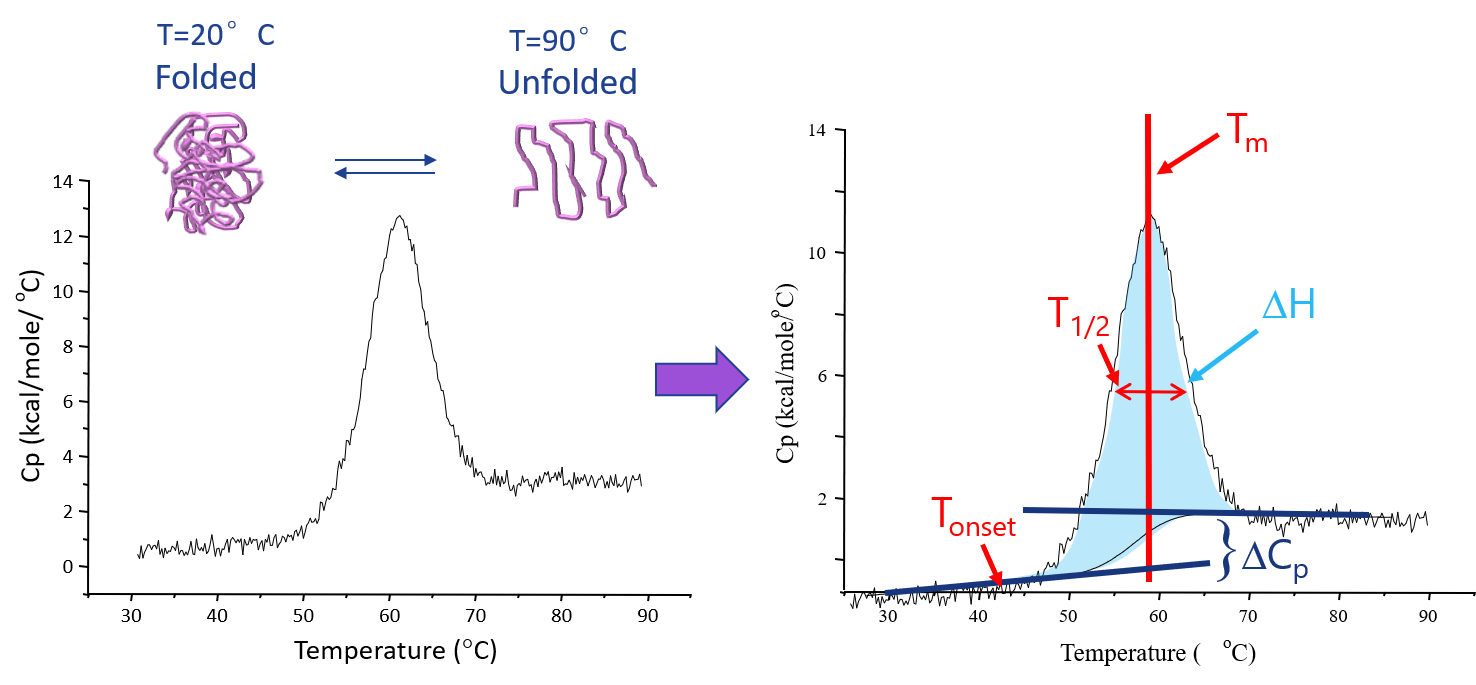
1. 能够检测出各种生物分子的热转变中点温度
2. 能够计算出热力学的参数(绝对值)
3. 能够同时分析多结构域的构象协同变化
4. 能够应用于相互作用分析
5. 能够评价多个结构域的复合物
1. 蛋白质工程: 药物稳定性改型
2. 纯化工艺开发: 筛选高得率、高稳定性纯化条件
3. 剂型设计: 筛选最稳定(最不稳定)剂型条件
4. 生物仿制药:仿制药与参比药生物一致性表征
服务热线:400-136-0316
电 话:18210288648/许经理
邮 箱:xhn@baks.com.cn
地 址:北京亦庄经济技术开发区科创十二街8号合众思壮2C-301

